-
:18964530232
-
:021-54379817


1.層狀金屬氧化物分類和制備:種類和合成方法多樣
1.1.層狀氧化物分類:數十種活性金屬元素,結構和種類繁多
鈉離子層狀氧化物中具有電化學活性的金屬元素多達數十種。層狀金屬氧化物材料的表達式為 NaxMO2(M 為過渡金屬元素)。在鋰離子電池中目前僅發現Mn、Co 和 Ni 三種金屬組成的鋰層狀氧化物可以實現可逆充放電,所以目前商業應用的鋰電正極材料包括鈷酸鋰(LiCoO2),NCM811,NCM622、NCM523 和錳酸鋰(LiMn2O4)等。而在鈉離子電池中,具有活性的層狀氧化物種類較多,Fe、Co、Ni、Mn、Cr、Cu 和 Ti 等元素均具有電化學活性且表現出多種性質。
圖表 1:鈉離子電池中常見的具有電化學活性的金屬元素
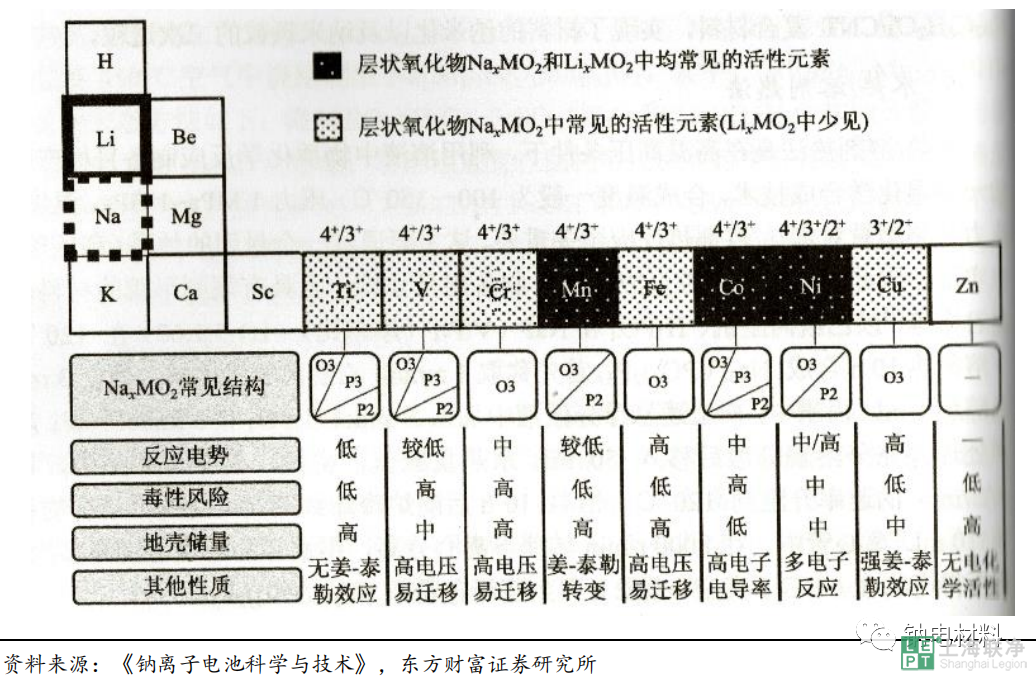
氧原子是層狀氧化物晶體結構的骨架。如圖 2 所示,在鈉離子的層狀金屬氧化物中,通常過渡金屬元素與周圍的六個氧形成的 MO6多面體層與 NaO6堿金屬層交替排布的層狀結構。所以,氧原子在層狀氧化物的晶體結構中主要承擔著晶格骨架的作用。

圖表 2:鈉離子電池層狀金屬氧化物晶體結構
過渡族金屬因為可以實現價態的變化,主要是提供電荷補償。如圖 3 所示,在實際的放電過程中,Na+離子從負極脫出,經由電解液穿過隔膜嵌入正極材料中,使得正極恢復至富鈉態。為保持電荷平衡,外電路會有相同的電子進行傳遞,對應的過渡族金屬會得到電子,并發生價態的變化,充電的過程則與之相反。
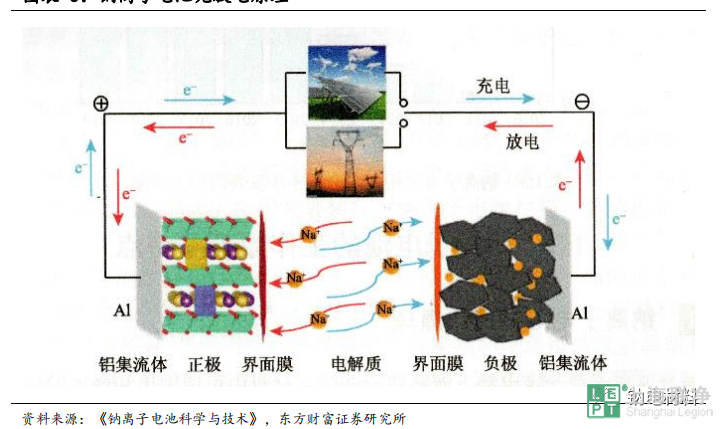
圖表 3:鈉離子電池充放電原理
根據晶體結構的差異,常見的層狀氧化物包括 P2 和 O3 型兩類。P2 和 O3根據過渡族金屬元素的組成又可以分為一元材料和多元材料。其中 O3 型多元材料種類目前在學術界和產業界研究最為充分,典型如中科院物理所胡勇勝團隊設計合成的 O3-Na0.9[Cu0.22Fe0.3Mn0.48]O2,和浙江鈉創新能源有限公司合成的O3-Na[Ni1/3Fe1/3Mn1/3]O2。
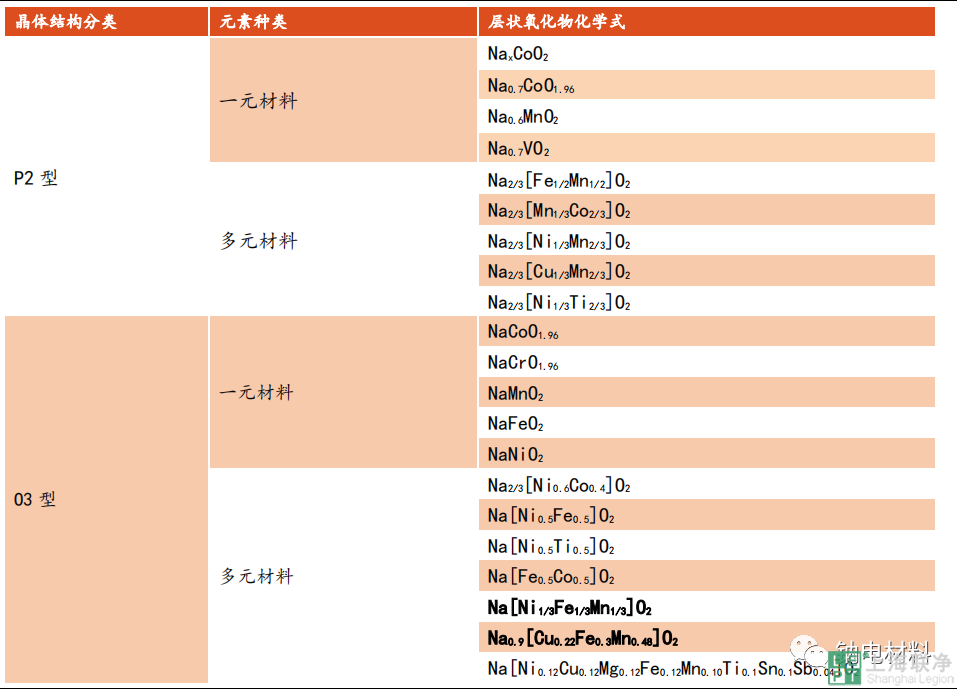
1.2.合成方法:固相法和液相法各有優劣
固相反應法流程簡單,是正極材料最常用的合成方法。該方法具有操作簡單、易于控制、工藝流程短和易工業化生產等優點。固相法中離子擴散的速度極其均勻性對產物的質量有非常重要的影響,因此經常通過降低粉末粒徑、提高粉末混合均勻性和適當提高燒結溫度等多重方法來加快離子擴散速度。固相法的主要劣勢就在于得到的樣品不能完全達到原子級別的均勻程度。如胡勇勝團隊就是以 Na2CO3為鈉源,與 CuO、Fe2O3和 Mn2O3混合,用固相法制備 O3-Na0.9[Cu0.22Fe0.3Mn0.48]O2。其大致過程是,首先將各種原材料按照摩爾比稱量,然后通過研磨混合均勻,期間可以加入一些分散劑增加混合程度。然后,將粉末在 900OC 空氣氣氛中燒結十余小時,自然冷卻后即可得到目標材料。
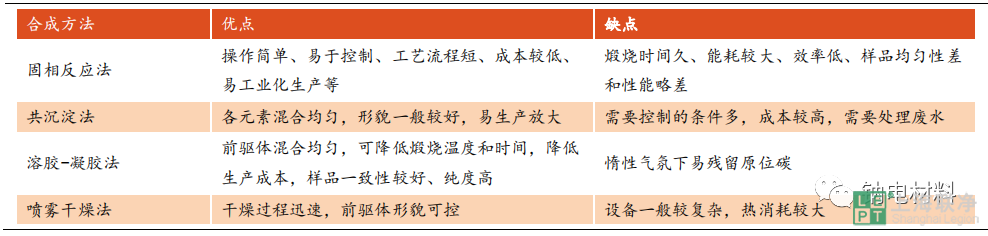
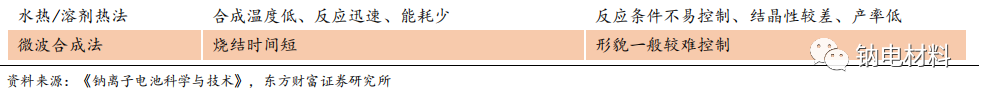
共沉淀法通過溶液內的反應可以實現原子級別的混合。共沉淀法也分為兩種, 其中第一種是一步沉淀法,即向原料溶液中添加適當的共沉淀劑,使溶液中已經混合均勻的各離子按照化學計量比共同沉淀出來,抽濾干燥后即可得到所需的樣品。第二種是先通過沉淀法獲得前驅體,再通過煅燒分解結晶得到最終產物。共沉淀法優勢在于其制備的前驅體顆粒尺寸形貌可控,顆粒的均勻性可以得到有效的保證,可以實現原子級別的混合程度。
上海交大的馬紫峰教授就是用共沉淀法制備了 Na[Ni1/3Fe1/3Mn1/3]O2。其主要步驟如下:先將 NiSO4.6H2O,FeSO4.7H2O 和 MnSO4.H2O 按照計量比混合,然后在溶液中加入 NaOH,之后將沉淀所得的[Ni1/3Fe1/3Mn1/3](OH)2沉淀過濾;然后,將干燥后的[Ni1/3Fe1/3Mn1/3](OH)2 前驅體與 Na2CO3混合,在 850OC 空氣中燒結制得Na[Ni1/3Fe1/3Mn1/3]O2。如表 5 所示,正極材料其他的合成方法還包括溶膠-凝膠法,噴霧干燥法,水熱/溶劑法和微波合成法等。
特別聲明:本站所轉載其他網站內容,出于傳遞更多信息而非盈利之目的,同時并不代表贊成其觀點或證實其描述,內容僅供參考。版權歸原作者所有,若有侵權,請聯系我們刪除。


掃描關注
上海聯凈官方微信
隨時了解最新資訊